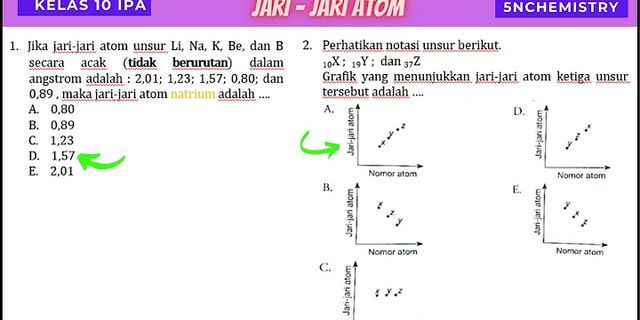
Pembahasan soal Kimia UN 2015 nomor 26 sampai dengan nomor 30 tentang:
Perhatikan gambar percobaan berikut!  Massa jenis air dianggap 1 g/cm3 dan kalor jenis air 4,2 J/g°C. HCl (aq) + NaOH (aq) → NaCl (aq) + H2O (l) ΔH reaksi untuk per mol H2O yang terbentuk adalah .... A. −50,40 kJ B. −51,50 kJ C. −54,60 kJ D. −55,44 kJE. −57,10 kJ Pada gambar percobaan di atas, setelah HCl dicampur dengan NaOH, terjadi kenaikan suhu sebesar 6 °C, yaitu dari 25 °C menjadi 31 °C. Ini menunjukkan bahwa reaksi yang terjadi adalah reaksi eksoterm (pelepasan panas). Adapun setelah 30 menit suhu turun kembali menjadi 25 °C, bukan berarti terjadi reaksi endoterm. Ini adalah proses penurunan suhu saja, karena reaksi sudah selesai. ΔH untuk reaksi eksoterm dirumuskan:  Tada negatif menunjukkan bahwa reaksi tersebut menghasilkan kalor atau eksoterm. Besarnya kalor yang dilepas pada reaksi tersebut adalah Q = m.c.Δt, [m = ρ.V] = ρ.V.c.Δt = 1 × 50 × 4,2 × 6 J = 1260 J Sekarang perhatikan persamaan reaksinya. Pada persamaan reaksi tersebut, semua koefisiennya sama, yaitu 1 sehingga mol H2O = mol HCl = M × V = 0,1 M × 25 ml = 2,5 mmol = 2,5 × 10−3 mol Dengan demikian, entalpi reaksi H2O adalah  Jadi, ΔH reaksi per mol H2O yang terbentuk adalah −50,40 kJ (A). Perhatikan peristiwa yang terjadi dalam kehidupan sehari-hari berikut ini!
E. (3) dan (4) 
Perdalam materi ini di Pembahasan Kimia UN: Termokimia. Pada percobaan reaksi antara logam aluminium dan asam sulfat sesuai persamaan reaksi: 2Al(s) + 3H2SO4(aq) → Al2(SO4)3(aq) + 3H2(g) Gas hidrogen ditampung dan diukur volumenya pada temperatur yang tetap. Data pengukuran tiap waktu sesuai tabel berikut:
E. 7,50 ml/detik Laju reaksi pembentukan gas hidrogen pada detik ke-15:   Laju reaksi pada detik ke-15 dan detik ke-30 mempunyai nilai yang sama. Berarti reaksi tersebut berjalan dengan kecepatan konstan (mempunyai nilai v yang sama setiap nilai t) Jadi, laju reaksi pembentukan gas hidrogen setelah detik 30 detik juga sama, yaitu 2,67 ml/detik (C). Perdalam materi ini di Pembahasan Kimia UN: Laju Reaksi. Dalam ruang 2 liter terdapat kesetimbangan: PCl5(g) ⇌ PCl3(g) + Cl2(g) Data percobaan pada keadaan kesetimbangan sebagai berikut:
Harga Kc berdasarkan data tersebut adalah ....  Konstanta kesetimbangan konsentrasi (Kc) adalah perbandingan konsentrasi produk terhadap konsentrasi reaktan dengan masing-masing konsentrasi dipangkatkan koefisiennya.  Sedangkan konsentrasi yang tersedia pada tabel adalah konsentrasi dalam satuan mol. Jadi, masing-masing harus dibagi V = 2 liter terlebih dahulu.  Jadi, harga Kc berdasarkan data tersebut adalah opsi (A). Perdalam materi ini di Pembahasan Kimia UN: Kesetimbangan Kimia. Perhatikan data percobaan berikut dengan teliti!
E. suhu Percobaan 2 dan 3 mempunyai konsentrasi dan suhu yang sama. Perbedaannya hanya pada ukuran partikel. Sedangkan ukuran partikel berhubungan dengan luas permukaan. Semakin halus ukuran partikel, semakin besar luas permukaannya sehingga reaksi berjalan lebih cepat. Jadi, perubahan laju reaksi pada percobaan 2 dan 3 dipengaruhi oleh luas permukaan (C). Simak Pembahasan Soal Kimia UN 2015 selengkapnya. Dapatkan pembahasan soal dalam file pdf di sini. Demikian, berbagi pengetahuan bersama Kak Ajaz. Silakan bertanya di kolom komentar apabila ada pembahasan yang kurang jelas. Semoga berkah.
© PT Zona Edukasi Nusantara, 2021. Kebijakan Privasi Ketentuan Penggunaan |

Pos Terkait
Periklanan
BERITA TERKINI
Toplist Popular
#2
#4
#6
#8
Periklanan
Terpopuler
Periklanan
Tentang Kami
Dukungan

Copyright © 2024 idkuu.com Inc.