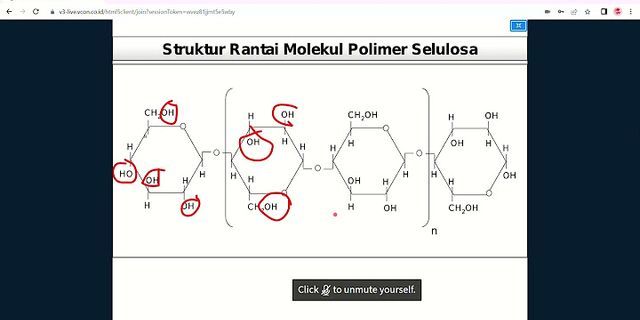
Sebuah protein dikatakan mengalami denaturasi ketika struktur tiga dimensinya (spasial) diubah karena beberapa alasan: panas, zat kimia, dll… Denaturasi protein terjadi ketika konformasi spasial atau struktur tiga dimensi protein hilang. Protein yang didenaturasi memiliki sifat yang berbeda dari protein yang sama dalam keadaan aslinya. Kami melihatnya misalnya saat kami memanaskan atau menggoreng telur dan kami memverifikasi bahwa putihnya, yang cair dan transparan, menjadi padat dan putih. Ini terjadi karena denaturasi ovalbumin. Dalam kasus lain, pemanasan menyebabkan jaringan menjadi lebih lembut. Misalnya, saat memasak daging, jaringan ikat yang dibentuk oleh protein yang disebut kolagen didenaturasi menjadi gelatin, yang hasilnya adalah daging yang lebih bisa dimakan. Karena enzim adalah molekul yang bersifat protein, jika kita mau, kita dapat mengubah sifatnya sehingga tidak bertindak. Jadi, padatan tersuspensi dari jus jeruk diendapkan karena aksi enzim pektinesterase, jadi jika Anda ingin jus tetap keruh, Anda harus menonaktifkan enzim dengan memanaskannya. Protein dapat ditemukan di semua organisme hidup. Masalah terjadi ketika protein menjadi terdenaturasi. Dalam Artikel ini, Anda akan belajar tentang perubahan dalam protein yang dikenal sebagai denaturasi. Denaturasi protein terdiri dari hilangnya struktur tiga dimensi karena faktor lingkungan yang berbeda, seperti suhu, pH, atau zat kimia tertentu. Hilangnya struktur mengakibatkan hilangnya fungsi biologis yang terkait dengan protein tersebut, baik itu enzimatis, struktural, transporter, dan lain-lain. Struktur protein sangat sensitif terhadap perubahan. Destabilisasi ikatan hidrogen esensial tunggal dapat mengubah sifat protein. Demikian pula, ada interaksi yang tidak sepenuhnya penting untuk memenuhi fungsi protein, dan, jika tidak stabil, tidak berpengaruh pada fungsi. PengertianDenaturasi protein adalah proses di mana protein mengalami perubahan struktural yang pada gilirannya menghasilkan perubahan fungsi, yang dapat menyebabkan hilangnya fungsi biologis secara total. Denaturasi protein dianggap sebagai jenis denaturasi biokimia, jenis lainnya adalah denaturasi asam nukleat (yang menyusun DNA dan RNA). Denaturasi biasanya disertai dengan perubahan sifat fisik-kimiawi protein, yang paling sering terjadi adalah hilangnya kelarutan, meskipun tidak selalu terjadi. Organisme hidup memerlukan banyak jenis molekul besar untuk bertahan hidup. Sangat sedikit molekul tersebut menjadi berbagai tujuan seperti protein. Protein adalah molekul besar yang terdiri dari rantai asam amino terlipat. Setiap protein memiliki bentuk unik dan fungsi berdasarkan bentuknya. Sangat mudah untuk berpikir tentang protein sebagai kunci yang cocok dengan membentuk gembok tertentu di sekitar tubuh. Protein berfungsi untuk mempercepat proses biologis, mengenali antibodi, mengatur proses fisiologis, menyediakan struktur, zat transportasi, mengatur gen, dan menanggapi sinyal di dalam dan di luar organisme. Protein berkisar dalam bentuk ukuran yang kecil seperti insulin yang hanya 51 asam amino ke yang panjang yang sangat besar seperti protein Titin yaitu panjang 26.926 asam amino. Tidak peduli ukuran mereka, mereka harus dilipat menjadi bentuk tertentu agar dapat berfungsi. Kadang-kadang sesuatu yang salah dan menyebabkan protein terkuak. Denaturasi adalah proses dimana protein kehilangan struktur terlipat dan berhenti berfungsi. Struktur ProteinDalam rangka untuk memahami denaturasi, sangat penting untuk memahami struktur protein. Protein terdiri dari asam amino. Para ilmuwan menggambarkan struktur protein dalam tingkatan. Keempat tingkatan adalah primer, sekunder, tersier, dan kuarterner. Struktur primer dari protein adalah urutan asam amino yang membentuk protein. Setiap protein memiliki urutan yang unik untuk asam amino. Jika asam amino rusak ini adalah protein tidak akan berfungsi dengan baik. Struktur sekunder protein menjelaskan pola berulang teratur lipatan awal yang ditemukan dalam protein. Ada dua jenis lipat pada tingkat ini, yang dikenal sebagai alfa heliks dan lempeng-beta. Sebuah alfa heliks adalah kumparan bentuk spiral yang terbentuk oleh ikatan hidrogen. Lempeng-beta terbentuk ketika dua rantai asam amino menyelaraskan dan membentuk pola wilayah datar atau berkerut. Struktur tersier protein menggambarkan bentuk protein ketika semua asam amino, heliks alfa, beta dan lembaran dilipat ke dalam struktur tertentu. Struktur kuartener menggambarkan protein yang terdiri dari dua subunit amino terlipat rantai asam yang datang bersama untuk membentuk satu protein akhir. Struktur primerIni adalah urutan asam amino yang membentuk protein tersebut. Asam amino adalah blok bangunan fundamental yang menyusun biomolekul ini dan ada 20 jenis berbeda, masing-masing dengan sifat fisik dan kimia tertentu. Mereka dihubungkan bersama melalui ikatan peptida. Struktur sekunderDalam struktur ini, rantai linier asam amino ini mulai melipat melalui ikatan hidrogen. Ada dua struktur sekunder dasar: α heliks, berbentuk spiral; dan lembaran terlipat β, ketika dua rantai linier disejajarkan. Struktur tersierIni melibatkan jenis gaya lain yang menghasilkan lipatan tertentu dari bentuk tiga dimensi. Rantai R dari residu asam amino yang membentuk struktur protein dapat membentuk jembatan disulfida, dan bagian hidrofobik dari protein menggumpal di bagian dalam, sedangkan bagian hidrofilik menghadapi air. Gaya van der Waals bertindak sebagai penstabil untuk interaksi yang dijelaskan. Struktur kuarterIni terdiri dari agregat unit protein. Ketika suatu protein didenaturasi, ia kehilangan struktur kuaterner, tersier dan sekunder, sedangkan yang primer tetap utuh. Protein yang kaya akan ikatan disulfida (struktur tersier) memberikan ketahanan yang lebih besar terhadap denaturasi. Faktor penyebab denaturasiDenaturasi protein terjadi ketika protein kehilangan struktur kuartener, tersier, dan sekunder. Pada dasarnya, protein menjadi membuka lipatan dan berhenti berfungsi. denaturasi Protein adalah penyebab oleh beberapa stres eksternal. Penyebab utama denaturasi protein mencakup paparan asam, basa, garam-garam anorganik, pelarut, atau panas. Pernahkah Anda menggoreng telur? Bila Anda menempatkan telur dalam panci memiliki kuning kuning cerah dikelilingi oleh protein yang jelas dikenal sebagai albumin, juga dikenal sebagai putih telur. Ketika telur terkena panas dalam panci albumin cepat berubah menjadi putih. Hal ini terjadi karena denaturasi protein bila terkena panas. Pernahkah Anda mengalami demam? Demam adalah baik karena mereka memberitahu kita sesuatu yang salah dalam tubuh dan meningkatkan suhu membantu untuk melawan penyerbu asing dalam tubuh. Namun, demam yang ekstrim bisa sangat berbahaya karena dapat menyebabkan protein dalam tubuh kita untuk mulai terdenaturasi. Demam dari 104 derajat atau lebih besar dapat menyebabkan denaturasi protein akan dimulai pada tubuh. Akhirnya, penting untuk dicatat bahwa sebagian besar protein denaturasi adalah permanen. Namun demikian, beberapa protein yang dapat melipat kembali dalam proses yang disebut renaturasi. Setiap faktor yang mengganggu kestabilan ikatan non-kovalen yang bertanggung jawab untuk menjaga struktur asli protein dapat menyebabkan denaturasi. Di antara yang paling penting kami dapat menyebutkan: 1. pHPada nilai pH yang sangat ekstrim, baik asam atau basa, protein dapat kehilangan konfigurasi tiga dimensinya. Kelebihan ion H + dan OH– dalam medium mendestabilisasi interaksi protein. Perubahan pola ion ini menyebabkan denaturasi. Denaturasi oleh pH dapat menjadi reversibel dalam beberapa kasus, dan dalam kasus lain tidak dapat diubah. 2. SuhuDenaturasi termal terjadi dengan meningkatnya suhu. Pada organisme yang hidup dalam kondisi lingkungan rata-rata, protein mulai tidak stabil pada suhu di atas 40 ° C. Jelas, protein organisme termofilik dapat menahan kisaran suhu ini. Peningkatan suhu diterjemahkan ke dalam peningkatan pergerakan molekul yang mempengaruhi ikatan hidrogen dan ikatan non-kovalen lainnya, yang mengakibatkan hilangnya struktur tersier. Peningkatan suhu ini menyebabkan laju reaksi yang lebih lambat, jika kita berbicara tentang enzim. 3. Zat kimiaZat polar – seperti urea – dalam konsentrasi tinggi memengaruhi ikatan hidrogen. Selain itu, zat nonpolar dapat memiliki konsekuensi yang serupa. Deterjen juga dapat mengganggu kestabilan struktur protein; namun, ini bukanlah proses yang agresif dan sebagian besar dapat dibatalkan. 4. Agen pereduksiΒ-Mercaptoethanol (HOCH2CH2SH) adalah zat kimia yang sering digunakan di laboratorium untuk mengubah sifat protein. Ini bertanggung jawab untuk mengurangi jembatan disulfida antara residu asam amino. Ini dapat menggoyahkan struktur protein tersier atau kuaterner. Agen pereduksi lain dengan fungsi serupa adalah dithiothreitol (DTT). Selain itu, faktor lain yang berkontribusi terhadap hilangnya struktur asli pada protein adalah logam berat dalam konsentrasi tinggi dan radiasi ultraviolet. DampakSaat terjadi denaturasi, protein kehilangan fungsinya. Protein berfungsi secara optimal ketika dalam keadaan asalnya. Kehilangan fungsi tidak selalu dikaitkan dengan proses denaturasi. Mungkin saja perubahan kecil pada struktur protein menyebabkan hilangnya fungsi tanpa menggoyahkan seluruh struktur tiga dimensi. Prosesnya mungkin tidak dapat diubah atau tidak. Di laboratorium, jika kondisinya terbalik, protein dapat kembali ke konfigurasi awal. RenaturasiSalah satu eksperimen paling terkenal dan konklusif tentang renaturasi dibuktikan di ribonuklease A. Ketika para peneliti menambahkan agen denaturasi seperti urea atau β-mercaptoethanol, protein tersebut terdenaturasi. Jika agen-agen ini dihilangkan, protein kembali ke bentuk aslinya dan dapat menjalankan fungsinya dengan efisiensi 100%. Salah satu kesimpulan terpenting dari penelitian ini adalah untuk menunjukkan secara eksperimental bahwa konformasi tiga dimensi protein ditentukan oleh struktur utamanya. Dalam beberapa kasus, proses denaturasi sama sekali tidak dapat diubah. Misalnya, saat kita memasak telur, kita menerapkan panas pada protein (yang utama adalah albumin) yang menyusunnya, putih menjadi padat dan tampak keputihan. Secara intuitif kita dapat menyimpulkan bahwa, meskipun kita mendinginkannya, itu tidak akan kembali ke bentuk awalnya. Dalam kebanyakan kasus, proses denaturasi disertai dengan hilangnya kelarutan. Ini juga mengurangi viskositas, kecepatan difusi dan lebih mudah mengkristal. Contoh denaturasiSalah satu contoh paling umum untuk menggambarkan denaturasi protein adalah memasak putih telur. Putih telur sebagian besar terdiri dari air dan albumin, sejenis protein. Saat suhu naik, protein dalam putih telur mengalami perubahan sifat, kehilangan kelarutannya dan putih telur menjadi cair dan transparan dan menjadi buram, putih dan padat. Contoh umum lainnya adalah denaturasi kasein dalam susu saat susu menjadi asam. Ini terjadi secara alami melalui fermentasi bakteri dan jamur, misalnya saat membuat yogurt. Anda juga dapat dengan mudah melihat apakah Anda menambahkan jus lemon ke segelas susu. Susu mengental saat kasein kehilangan kelarutannya. Ringkasan
|

Pos Terkait
Periklanan
BERITA TERKINI
Toplist Popular
#2
#4
#6
#8
Periklanan
Terpopuler
Periklanan
Tentang Kami
Dukungan

Copyright © 2024 idkuu.com Inc.